●冠病19疫情
美研究团队在《新英格兰医学杂志》发表莫德纳疫苗的第一阶段临床实验报告。报告说,接种了两剂疫苗的所有45名健康志愿者体内都产生了大量的病毒抗体,超过了已经康复的患者体内的平均抗体水平。
傅慧云 整理
(芝加哥综合电)初步研究显示,美国生物技术公司莫德纳(Moderna)与美国国家卫生研究院合作开发的冠病疫苗,具有安全性并可激发所有参与测试者产生免疫反应。莫德纳随即宣布本月底启动对该疫苗的最后阶段临床实验。
美国国家过敏和传染病研究所研究团队周二在《新英格兰医学杂志》上发表莫德纳疫苗的第一阶段临床实验报告。报告说,接种了两剂疫苗的所有45名健康志愿者体内都产生了大量的病毒抗体,超过了已经康复的患者体内的平均抗体水平。
没有志愿者出现严重副作用,但半数以上的志愿者称有轻度或中度反应,比如乏力、头痛、发冷、肌肉疼痛或注射部位疼痛。这些反应更有可能出现在接种第二剂疫苗后,以及接受最高剂量注射的志愿者身上。
美国国家过敏和传染病研究所所长福奇说,这一结果是个“好消息”,并指出该研究没有发现严重不良反应,而且疫苗产生了“相当高”水平的杀灭或中和病毒的抗体。
福奇说:“如果疫苗能引起与自然感染相当的反应,那就成功了。这也是我们为什么对这一结果感到非常高兴。”
莫德纳是在3月16日率先对冠病疫苗展开人体实验,那时距离冠病病毒基因序列公布仅66天。5月,莫德纳公布了第一阶段实验的“中期结果”,显示八名志愿者体内出现了冠病抗体。莫德纳随后启动了第二阶段临床实验,该阶段的研究结果还未公布。
若获监管局批准年产可高达10亿剂
不过,随着疫苗的安全性和成效在第一阶段实验中获得认可,莫德纳周二宣布将在7月27日启动第三也是最后阶段的临床实验,以测试该疫苗对3万名志愿者在真实世界中的有效性。若获得监管局批准,莫德纳称可从明年起每年生产5亿至10亿剂疫苗。
无论如何,研究人员将对志愿者展开长达两年的跟踪调查,以确定他们是否免疫或如果受到感染是否能预防发病。即使志愿者病发,只要没有出现严重病情,那该疫苗仍被视为有效。
就在疫苗研究传来好消息的当儿,美国的疫情却持续恶化。约翰霍普金斯大学的统计显示,全美周二出现了6万多起新病例,累计超过343万起,当中13万6000多人病逝。
亚拉巴马、佛罗里达和北卡罗来纳州周二刷新了州内单日最高死亡纪录。佛州当天有133人死于冠病,累计达到4500多人。亚拉巴马和北卡州分别有40和30起死例,累计都超过1100起。得克萨斯州则出现1万零745起新病例,再破该州单日纪录。
尽管患者持续增加,但美国总统特朗普仍坚称,继续关闭学校是“严重的错误”。传染病专家福奇则说,是否要重开学校应视各地区疫情而定,地方官员应自行决定。

 国际特稿:白罗斯反击欧盟移民沦为棋子
国际特稿:白罗斯反击欧盟移民沦为棋子 美医学专家:“清零”策无法根除冠病
美医学专家:“清零”策无法根除冠病 韩国前总统“光州屠夫”全斗焕病逝
韩国前总统“光州屠夫”全斗焕病逝 专家:多国悄悄展开军备竞赛
专家:多国悄悄展开军备竞赛 七国集团吁采紧急行动对抗新病毒
七国集团吁采紧急行动对抗新病毒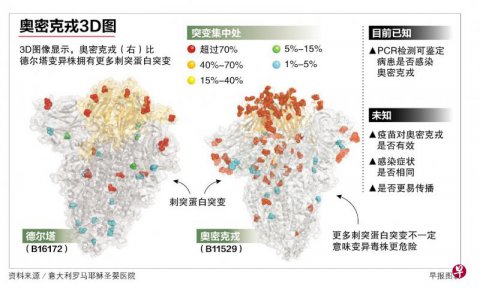 全球加紧研究奥密克戎 暂不能确定症状
全球加紧研究奥密克戎 暂不能确定症状 面临新毒株威胁 欧洲各国不敢掉以轻心
面临新毒株威胁 欧洲各国不敢掉以轻心 多国对南非实施入境限制 旅客涌向机场
多国对南非实施入境限制 旅客涌向机场