中国国药集团董事长刘敬桢周二(20日)说,国药集团中国生物的两支冠病灭活疫苗,均纳入了紧急使用的范围,目前已做好大规模生产准备工作,国药明年冠病疫苗产能将达到10亿剂以上。
据路透社报道,他在联防联控机制发布会上说:“当前冠病灭活疫苗正在全力冲刺阶段,国药集团中国生物疫苗研发是万里长征还剩最后一公里,在III期临床试验取得安全性和保护力数据以后,疫苗经审评获批就可以上市。”
他指出,目前中国生物已做好大规模生产准备工作,北京生物制品研究所、武汉生物制品研究所两个冠病疫苗P3生产工厂已经建设完成,明年产能将达到10亿剂以上,能够保证安全充足的疫苗供应。
他介绍,国药集团中国生物所属的北京生物制品研究所和武汉生物制品研究所这两款灭活疫苗现在正在阿联酋、巴黎、约旦、秘鲁、阿根廷、埃及等十个国家开展III期临床试验,目前已经接种五万余人,总共接种者将达到六万余人。现在已经有几十个国家向国药集团中国生物提出冠病疫苗的需求。
中国科技部社会发展科技司副司长田保国同一场合说,目前中国灭活疫苗和腺病毒载体疫苗两种技术路线共四个疫苗进入了III期临床试验,总体上进展顺利,截止到目前共计接种了约六万名受试者,未收到严重不良反应的报告,初步显示了良好的安全性。
他说,中国科研攻关组布局了灭活疫苗、重组蛋白疫苗、腺病毒载体疫苗、减毒流感病毒载体疫苗和核酸疫苗五个技术路线并行研发,每条技术路线都有进入临床研究阶段的疫苗,已有13个疫苗进入了临床试验。
他指出,目前中国的疫苗研发工作总体上是处于领先地位。III期临床试验结果是验证疫苗保护力国际公认的有效性的指标,在目前中国冠病疫情得到有效控制、不具备开展III期临床试验条件的情况下,如何选择合适的地区和受试人群,以及顺利地组织实施III期临床试验,是目前开展III期临床试验面临的主要问题。
田保国并称,通过对超过八万条高质量的病毒基因组序列进行比较分析研究,结果表明病毒变异不大,属于正常范围内的变异积累,没有对疫苗研发造成实质性的影响。
国家药监局药审中心首席审评员王涛说,药监局将依法依规特事特办,第一时间完成疫苗审批保供应。
中国已加入“冠病疫苗实施计划”(COVAX),外交部国际司二级巡视员赵星说,下一步会利用实施计划的平台加强同其他国家和国际组织的合作,另一方面也支持中国的疫苗企业参加到实施计划中,同实施计划的发起方一起向发展中国家提供疫苗。

 江西“挖矿”余波震荡龚建华投案受查
江西“挖矿”余波震荡龚建华投案受查 新闻人间:徐旭东 蓝绿通吃挨红罚
新闻人间:徐旭东 蓝绿通吃挨红罚 处分七名干部 安阳反思“狗咬人”事件
处分七名干部 安阳反思“狗咬人”事件 下午察:大汪离婚变成独统战场?
下午察:大汪离婚变成独统战场? 在吉林越狱潜逃41天 朝鲜脱北者被捕
在吉林越狱潜逃41天 朝鲜脱北者被捕 央行:微信码“不能用于经营收款”系误读
央行:微信码“不能用于经营收款”系误读 江浙沪多地发生本土疫情 上海暂停跨省旅游
江浙沪多地发生本土疫情 上海暂停跨省旅游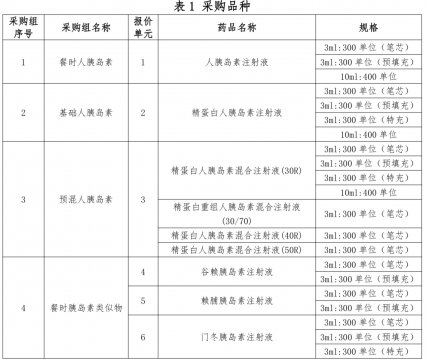 胰岛素首进全国药品集采:明日开标
胰岛素首进全国药品集采:明日开标